


Les molécules d'anticorps ont maintenant fait leur preuve en pratique clinique et sont à la base de nombreux traitements. Cependant, la plupart des cibles faciles ont été exploitées et la prochaine génération d'anticorps monoclonaux humains devra cibler des molécules complexes comme les protéines intégrales de membrane et/ou nécessitera des propriétés particulières (agoniste, antagoniste, etc.) pour ouvrir de nouvelles voies thérapeutiques. L'équipe possède une expertise de longue date dans l'ingénierie des protéines, en particulier dans le domaine des anticorps. Nous capitalisons sur cette expertise pour développer des molécules originales et innovantes à base d'anticorps pour des applications in vitro et in vivo.
Objectif 1. Conception et construction de bibliothèques synthétiques d’anticorps
Les anticorps sont maintenant reconnus comme un élément clé des thérapies ciblées contre le cancer. Le développement des anticorps monoclonaux a rapidement évolué au cours des 20 dernières années pour devenir un pipeline plus robuste et efficace. Cela a été accompli en particulier par le développement des technologies de display (notamment la présentation sur phages; G. Winter et G. Smith, prix Nobel de chimie 2018) et la construction de bibliothèques d’anticorps humains. Il y a 15 ans, nous avons choisi de concentrer nos travaux sur le développement de bibliothèques d'anticorps humains entièrement synthétiques, car nous pensons que cela permet un pipeline plus efficace en raison de la plus grande homogénéité des bibliothèques obtenues. Les bibliothèques développées par l'équipe sont les seules bibliothèques académiques d'anticorps humains disponibles pour la recherche en France. Nous continuons à développer de nouvelles bibliothèques synthétiques humaines innovantes basées sur des analyses structure-fonction des répertoires humains dans le but d'améliorer la diversité fonctionnelle et la développabilité des clones, ainsi qu'un pipeline amélioré pour la caractérisation rapide et directe des clones en format IgG.
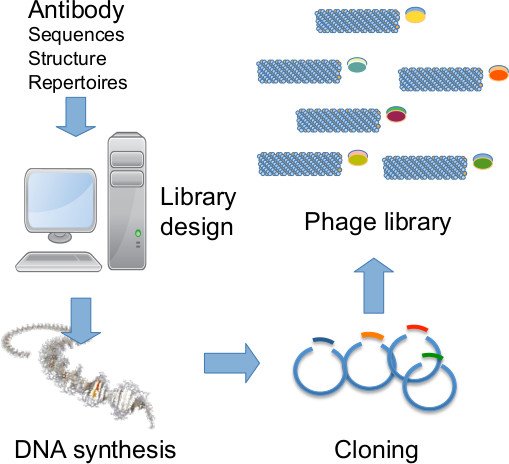
Objectif 2. Anticorps en tant que biocapteurs et inhibiteurs
Les anticorps sont hautement spécifiques de leur cible et peuvent être obtenus contre pratiquement n'importe quelle partie d'une protéine, en particulier contre les zones planaires où des interactions protéiques ont souvent lieu et qui sont difficiles à cibler avec de petites molécules organiques ou des peptides. Cette spécificité et cette affinité élevées sont couramment utilisées dans les laboratoires de recherche et font des anticorps l’outil protéomique le plus répandu. L'extension de l'utilisation d'anticorps dans la cellule est l'objectif principal de l'approche des intracorps, qui propose d'exprimer des fragments d'anticorps dans la cellule pour inhiber et moduler les fonctions des protéines. Cependant, les anticorps naturels ne sont pas adaptés à l'environnement intracellulaire en raison de leur grande taille et du fait que l'environnement réducteur du cytoplasme empêche la formation des ponts disulfure et donc le repliement correct des anticorps. Nos travaux sur des bibliothèques synthétiques humaines optimisées nous permettent d’isoler des fragments d’anticorps d’une stabilité exceptionnelle et capables de se replier dans l’environnement réducteur du cytoplasme cellulaire. Nous nous concentrons actuellement sur l'utilisation d'intracorps pour cibler les modifications post-traductionnelles dans les cellules et à leur utilisation dans des modèles précliniques.
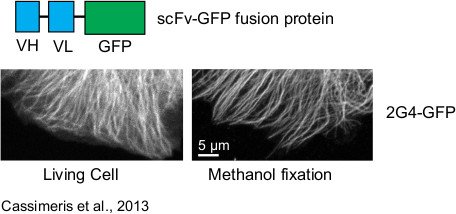
Objectif 3. Anticorps innovants pour le ciblage tumoral
La plupart des anticorps utilisés jusqu'à présent en clinique ont été obtenus par immunisation. Ceci a pour inconvénient de limiter la diversité potentielle des molécules obtenues car il est presque impossible de produire des anticorps contre les épitopes conservés au cours de l'évolution. De plus, les technologies de display in vitro permettent d'isoler directement des molécules entièrement humaines et de développer des pipelines de sélection adaptés à l'identification d'anticorps monoclonaux dotés de propriétés de liaison originales. En combinant nos connaissances en matière de conception d'anticorps synthétiques et de sélection in vitro, nous cherchons actuellement à développer des anticorps humains mieux adaptés au micro-environnement de la tumeur. Notre objectif principal est de développer des anticorps monoclonaux offrant une efficacité de ciblage améliorée, même dans les cas fréquents d'expression de la cible par le tissu sain. Cela permettra d'optimiser le rapport efficacité / toxicité afin de produire des anticorps monoclonaux améliorés pour la thérapie humaine.
Les molécules d'anticorps ont maintenant fait leur preuve en pratique clinique et sont à la base de nombreux traitements. Cependant, la plupart des cibles faciles ont été exploitées et la prochaine génération d'anticorps monoclonaux humains devra cibler des molécules complexes comme les protéines intégrales de membrane et/ou nécessitera des propriétés particulières (agoniste, antagoniste, etc.) pour ouvrir de nouvelles voies thérapeutiques. L'équipe possède une expertise de longue date dans l'ingénierie des protéines, en particulier dans le domaine des anticorps. Nous capitalisons sur cette expertise pour développer des molécules originales et innovantes à base d'anticorps pour des applications in vitro et in vivo.